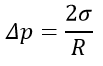Относительная молекулярная (атомная) масса:
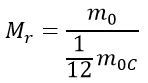
Mr – относительная молекулярная (атомная) масса вещества определяется по таблице Менделеева;
m0С – масса молекулы (атома) углерода C, а.е.м.;
m0 – масса молекулы (атома) вещества, а.е.м.
Основное уравнение молекулярно- кинетической теории (давления идеального газа):
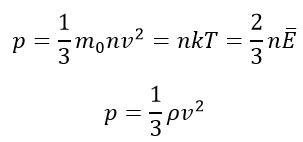
m0 — масса молекулы газа, кг;
n — концентрация молекул газа, м-3;
v — скорость движения молекул, м/с
Средняя кинетическая энергия:
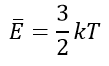
Масса молекулы:
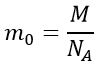
Абсолютная температура:
T=t+273
Уравнение Менделеева- Клайперона (состояние идеального газа):
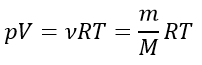
p – давление газа, Па;
V – объем газа, м3;
ν – количество веществ, моль
m – масса газа, кг;
M – молярная масса, кг/моль;
T – температура газа, К.
R – универсальная газовая постоянная
Формула для определения количества вещества:
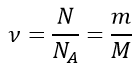
Концентрация:
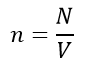
Масса вещества:
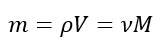
Количество молекул:
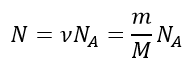
Количество атомов:
![]()
k – число атомов в молекуле
Скорость движения частиц:
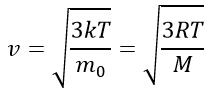
Смесь газов в одном сосуде:
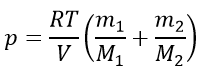
Открыли кран соединяющий сосуды:
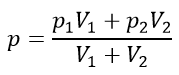
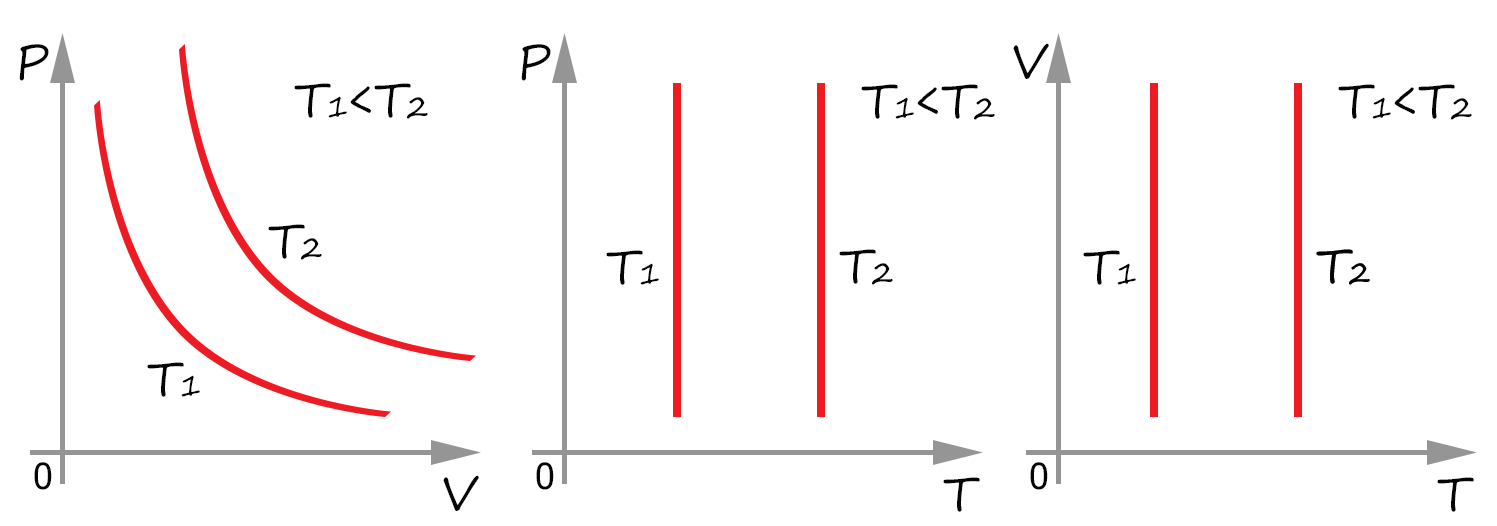
Закон Бойля-Мариотта (изотермический процесс):
![]()
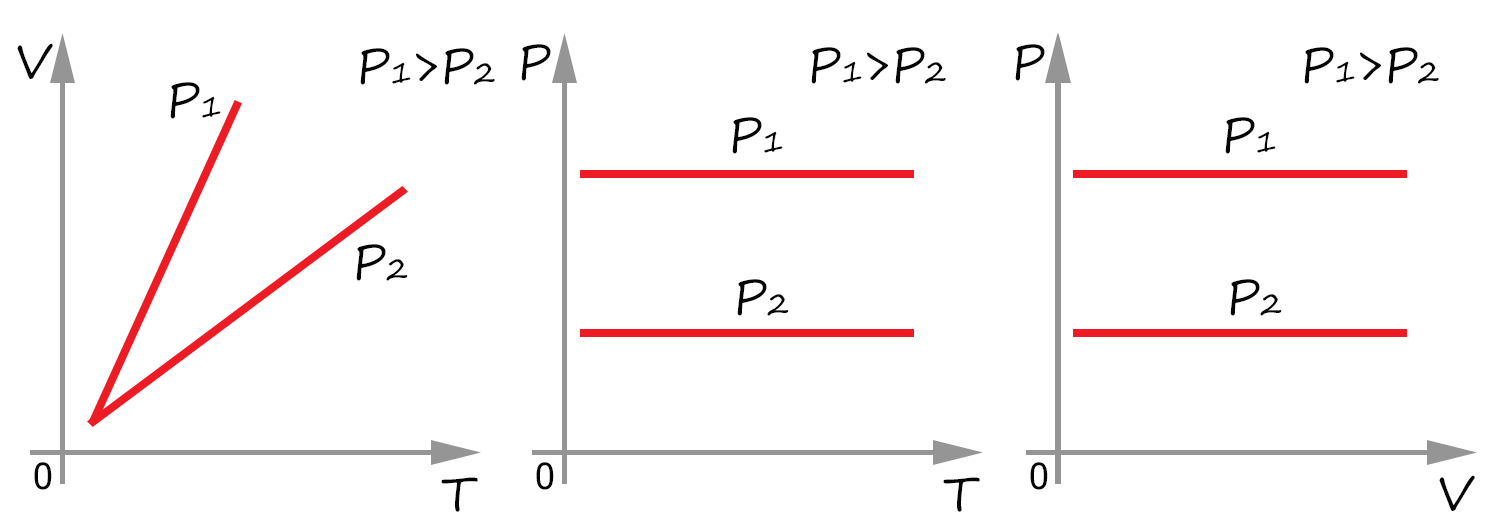
Закон Люсака (изобарный процесс):
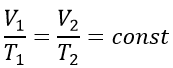
Закон Шарля (изохорный процесс):
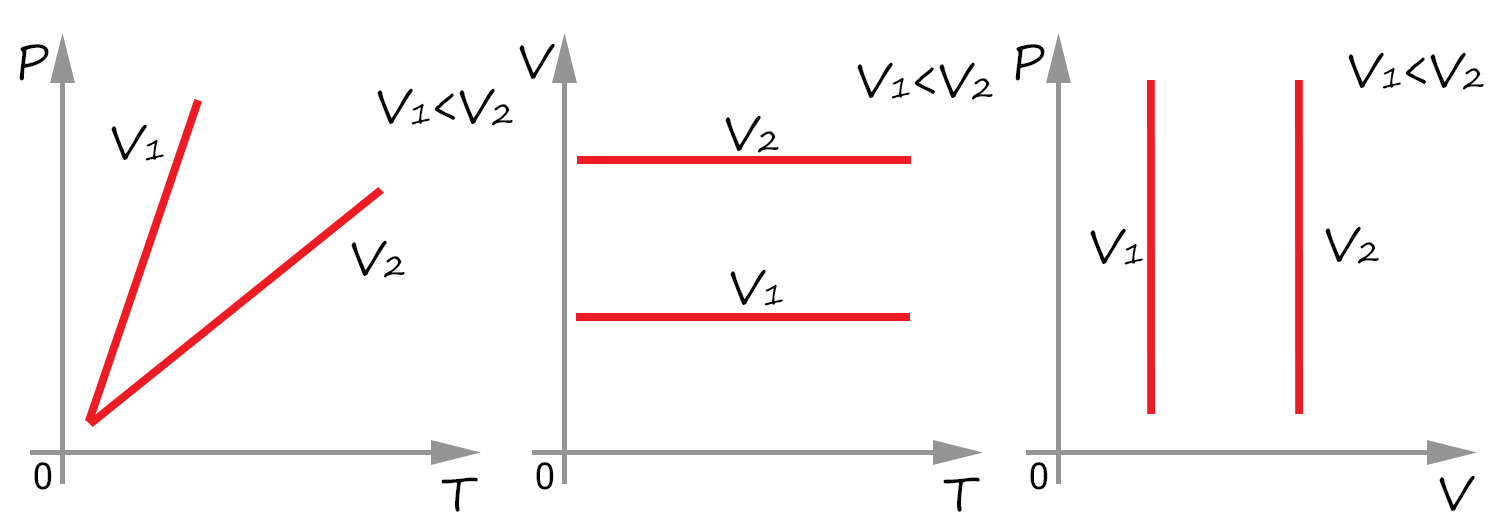
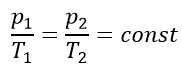
Уравнение Клайперона:
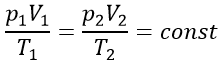
Работа газа:
![]()
Уравнение первого закона термодинамики:
![]()
U – внутренняя энергия;
Q – количество теплоты;
А – работа внешних сил
КПД тепловой машины:
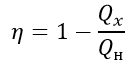
КПД идеальной тепловой машины:
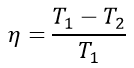
Максимальное КПД (Сади Карно):
![]()
Давление под искривленной поверхностью: