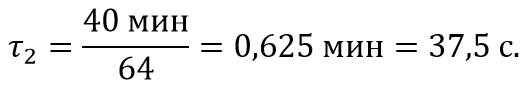Правило Вант-Гоффа (голландский химик 1852-1911 гг.) формулировка:
в интервале температур от 0°С до 100°С при повышении температуры на каждые 10° С скорость многих химической реакции увеличивается в 2-4 раза.
В виде математической формулы правило Вант-Гоффа выражается следующей зависимостью
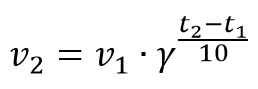
где
v1 и v2 — скорости реакции при температурах t1 и t2;
t1 – начальная температура;
t2 – конечная температура;
γ – температурный коэффициент от 2 до 4 (непостоянен и вычисляется экспериментально – опытным путём), который показывает во сколько раз возрастает скорость химической реакции при повышении температуры на 10°С.
Химические реакции с участием молекул сложной формы (таких как, белков) не подчиняются правилу Вант-Гоффа.
Уравнение Аррениуса, математическое выражение:
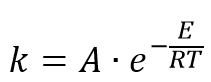
K – константа скорости реакции;
А — коэффициент Аррениуса;
Е — энергия активации;
R — универсальная газовая постоянная;
Т — температура, К.
Задача
При температуре 20 градусов некоторая реакция заканчивается за 40 минут. Вычислите за какое время закончится эта реакция при температуре 80 градусов. Температурный коэффициент скорости реакции равен 2.
Дано
τ1=40 мин.
t1=20 0C
t2=80 0C
γ=2
τ2-?
Решение
Определим во сколько раз возрастет скорость реакции при увеличении температуры с 20 до 80 градусов.
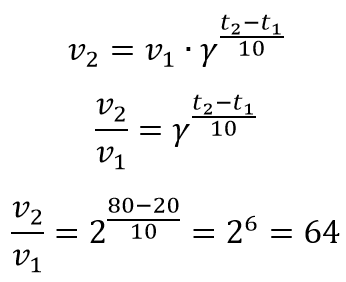
Найдем за какое время закончится эта реакция